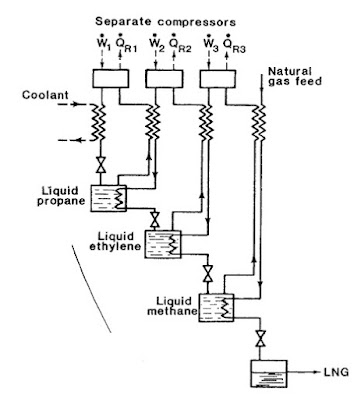
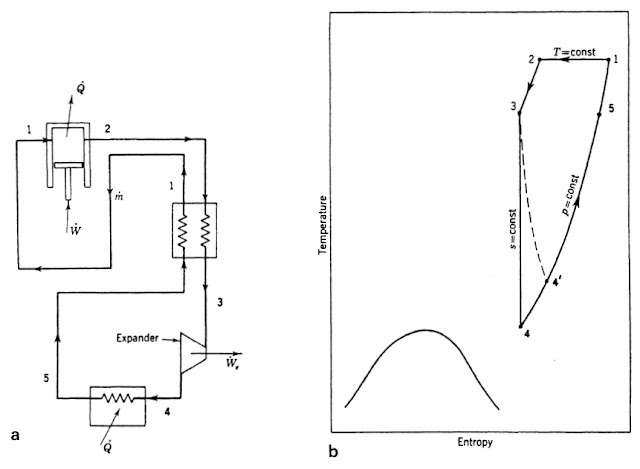
Orto-paravodonik konverzija
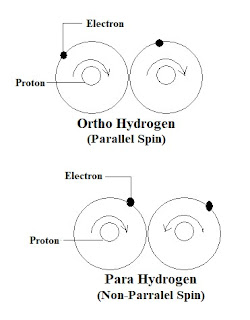
Struktura ortovodonika i paravodonika. Dva aranžmana za pretvaranje ortovodonika u paravodonik. Godine 1932, fizičar Verner Hajzenberg dobio je Nobelovu nagradu „za stvaranje kvantne mehanike, čija je primena, između ostalog, dovela do otkrića alotropnih oblika vodonika“. Bio je glavni naučnik u nemačkom programu nuklearnog oružja tokom Drugog svetskog rata. Takođe je bio ključan u planiranju prvog zapadnonemačkog nuklearnog reaktora u Karlsrueu, zajedno sa istraživačkim reaktorom u Minhenu, 1957. Likvifikacija vodonika sa sobom donosi dodatni aspekt koji se ne sreće kod drugih kriogenih tečnosti. Vodonik postoji u dva oblika, ortovodonik i paravodonik, a ravnotežna koncentracija između njih zavisi od temperature vodonika. Na sobnoj temperaturi, ova koncentracija je oko 75% ortovodonika i 25% paravodonika (generalno označenog kao normalni vodonik), dok je ravnotežna koncentracija na normalnoj tački ključanja vodonika skoro sav paravodonik. Kada je ...